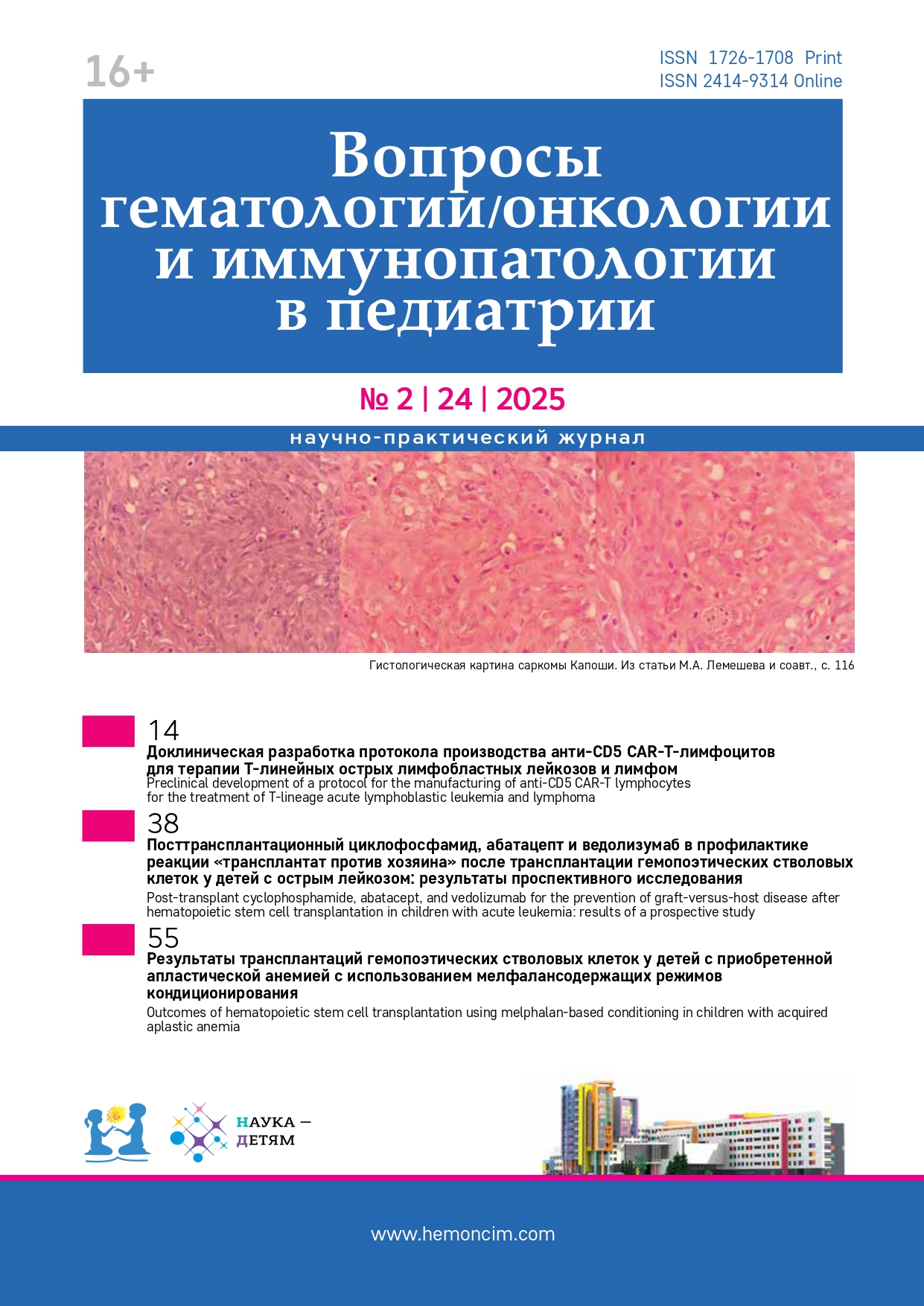
Влияние двух стратегий трансфузии эритроцитсодержащих компонентов крови на исходы и частоту анемии после выписки у недоношенных детей с экстремально низкой массой тела при рождении
- Авторы: Шарафутдинова Д.Р.1,2, Балашова Е.Н.1, Пучкова А.А.1, Дегтярева А.В.1,2, Киртбая А.Р.1,2, Лутфуллина Р.А.1, Цечоева Т.К.1, Козловская А.А.1, Ионов О.В.1,2
-
Учреждения:
- ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова» Минздрава России
- ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Сеченовский Университет)
- Выпуск: Том 24, № 2 (2025)
- Страницы: 86-94
- Раздел: ОРИГИНАЛЬНЫЕ СТАТЬИ
- Статья получена: 27.02.2025
- Статья одобрена: 22.04.2025
- Статья опубликована: 08.09.2025
- URL: https://hemoncim.com/jour/article/view/963
- DOI: https://doi.org/10.24287/1726-1708-2025-24-2-86-94
- EDN: https://elibrary.ru/LZDMEC
- ID: 963
Цитировать
Полный текст
Аннотация
Недоношенные новорожденные с экстремально низкой массой тела при рождении являются основной категорией детей, получающих одну трансфузию донорских эритроцитсодержащих компонентов (ЭСК) крови и более в течение неонатального периода для коррекции анемии. Существующие стратегии переливания подразделяются на либеральную, направленную на поддержание более высокого уровня гемоглобина, и рестриктивную, при которой трансфузия назначается на более низких уровнях гемоглобина. Цель: сравнить неонатальные исходы и частоту развития анемии после выписки в течение 24 месяцев жизни у детей с экстремально низкой массой тела при рождении, получавших трансфузии донорских ЭСК крови по либеральной и рестриктивной стратегиям. Исследование одобрено комиссией по этике биомедицинских исследований (протокол №12 от 17 ноября 2016 г.) и утверждено решением ученого совета (протокол №19 от 29 ноября 2016 г.) ФГБУ «НМИЦ АГП им. акад. В.И. Кулакова» Минздрава России. На базе клинических отделений Института неонатологии и педиатрии ФГБУ «НМИЦ АГП им. акад. В.И. Кулакова» Минздрава России проведено одноцентровое ретроспективное когортное исследование. Пациенты были разделены на 2 группы: дети, которым проводились трансфузии донорских ЭСК крови по либеральной (1-я группа) и рестриктивной (2-я группа) стратегиям. Определяли частоту таких исходов, как ретинопатия недоношенных (РН) ≥ III степени, некротизирующий энтероколит (НЭК) ≥ II степени, бронхолегочная дисплазия (БЛД), внутрижелудочковые кровоизлияния (ВЖК) ≥ II степени, перивентрикулярная лейкомаляция (ПВЛ); анемия после выписки в скорректированных возрастах (СВ) 1, 3, 6, 12 18 и 24 месяца жизни. Гестационный возраст новорожденных составил от 24 до 28 недель. В 1-й и 2-й группах частота переливания ЭСК крови составила 136/164 (82,9%) против 149/216 (68,9%), медиана объема переливания – 29,3 мл/кг (IQR 17,5–51,8 мл/кг) против 19,5 мл/кг (IQR 15,0–29,5 мл/кг), р < 0,05. Статистически значимых отличий в частоте БЛД, ВЖК ≥ II степени, ПВЛ, РН ≥ III степени в исследуемых группах не выявлено. Частота НЭК ≥ II степени во 2-й группе была выше в 1,6 раза, чем в 1-й группе. Частота анемии после выписки была ниже в 1-й группе по сравнению со 2-й группой в СВ 1 и 3 месяца (в возрасте 1 месяца – 32/72 (44,4%) против 106/166 (63,8%), р = 0,026, в возрасте 3 месяцев – 28/72 (38,9%) против 90/166 (54,2%), р = 0,042). Тяжелая анемия после выписки не регистрировалась ни в одной группе. После СВ 6 месяцев жизни разницы в частоте анемии между группами не наблюдалось. Применение рестриктивной стратегии гемотрансфузии не приводит к клинически значимому увеличению частоты РН ≥ III степени, БЛД, ПВЛ, ВЖК ≥ II степени, а также анемии после 6 месяцев жизни. Однако шансы развития НЭК ≥ II степени в группе рестриктивной стратегии были выше в 1,6 раза, чем в либеральной, что требует дополнительного анализа.
Полный текст
В течение неонатального периода более чем в 80% случаев недоношенным детям с очень низкой и экстремально низкой (ЭНМТ) массой тела при рождении требуется проведение трансфузии донорских эритроцитсодержащих компонентов (ЭСК) крови в связи с развитием анемии [1-3]. Существуют 2 основные стратегии переливания донорских ЭСК крови: либеральная и рестриктивная. Либеральная стратегия направлена на поддержание более высокого уровня гемоглобина, тогда как рестриктивная стратегия является более выжидательной и предполагает проведение трансфузий при более низком уровне гемоглобина.
Несмотря на высокую частоту переливания донорских ЭСК крови недоношенным детям, потенциальные преимущества и/или отрицательное влияние дополнительного переливания крови до конца не изучены. На сегодня проведены и опубликованы результаты крупных рандомизированных контролируемых исследований (РКИ), сравнивающих либеральную и рестриктивную стратегии трансфузий донорских ЭСК крови у детей с ЭНМТ при рождении, анализирующих отдаленные исходы, преимущественно неврологические [1, 4]. Эти исследования не выявили значимых различий в когнитивном развитии детей в скорректированном возрасте (СВ) 22-26 месяцев жизни [1-4]. Тем не менее в проведенных исследованиях есть ряд ограничений. В частности, в них не оценивались частота развития и тяжесть анемии у исследуемых пациентов после выписки.
Цель данного исследования - сравнить неонатальные исходы и частоту развития анемии после выписки в течение 24 месяцев жизни у детей с ЭНМТ при рождении, получавших трансфузии донорских ЭСК крови по либеральной и рестриктивной стратегиям.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
На базе клинических отделений Института неонатологии и педиатрии ФГБУ «НМИЦ АГП им. акад. В.И. Кулакова» Минздрава России проведено одноцентровое двойное ретроспективное когортное исследование. Исследование одобрено комиссией по этике биомедицинских исследований (протокол №12 от 17 ноября 2016 г.) и утверждено решением ученого совета (протокол №19 от 29 ноября 2016 г.) ФГБУ «НМИЦ АГП им. акад. В.И. Кулакова» Минздрава России.
Критерии включения: недоношенные новорожденные с ЭНМТ при рождении, наличие информированного согласия, подписанного законными представителями пациентов.
Критерии исключения: врожденные пороки развития, требующие хирургической коррекции в неонатальном периоде, наследственные болезни обмена, внутриутробные гемотрансфузии, тяжелая форма гемолитической болезни новорожденных, синдром анемии-полицитемии при монохориальных беременностях, недоношенные дети, умершие до проведения первой гемотрансфузии.
Выполнен анализ 380 случаев выхаживания недоношенных детей с ЭНМТ, рожденных в период с 2014 по 2023 г. в ФГБУ «НМИЦ АГП им. акад. В.И. Кулакова» Минздрава России.
С учетом исторически сложившихся периодов, связанных с изменениями показаний к проведению трансфузий донорских ЭСК крови в НМИЦ АГП им. акад. В.И. Кулакова, выделено 2 группы детей:
- 1-я группа - недоношенные дети с ЭНМТ, которым проводились трансфузии донорских ЭСК крови по либеральной стратегии - до апреля 2018 г.;
- 2-я группа - недоношенные дети с ЭНМТ, которым проводились трансфузии донорских ЭСК крови по рестриктивной стратегии - с апреля 2018 г.
На 1-м этапе проводилась оценка неонатальных исходов при выписке из стационара, на 2-м этапе - оценка частоты и тяжести анемии после выписки.
Конечными точками были следующие: оценка частоты развития таких исходов, как ретинопатия недоношенных (РН) > III степени, некротизирующий энтероколит (НЭК) > II степени, бронхолегочная дисплазия (БЛД), внутрижелудочковые кровоизлияния (ВЖК) > II степени, постгеморрагическая гидроцефалия, перивентрикулярная лейкомаляция (ПВЛ); анемия после выписки и в СВ 1, 3, 6, 12, 18, 24 месяца жизни.
На различных этапах из исследования выбыли 142 ребенка. Причиной исключения явились летальный исход до выписки из стационара (n = 23), отсутствие данных о наблюдении и результатах обследований детей после выписки (п = 119).
Формирование выборки новорожденных детей, включенных в исследование, представлено на рисунке 1.
Критериями диагностики ранней анемии недоношенных являлось снижение уровня гемоглобина и/или гематокрита (Ht) более чем на 2 стандартных отклонения от средних значений этих показателей для данного постнатального возраста [5]. После выписки из стационара и до СВ 6 месяцев критерием анемии являлось снижение гемоглобина менее 100 г/л, после 6 месяцев до 2 лет - менее 110 г/л. [6, 7]. Анемия тяжелой степени диагностировалась при гемоглобине < 70 г/л [8, 9].
Показания для проведения трансфузии донорских эритроцитсодержащих компонентов крови
Проведение трансфузий по либеральной стратегии не имеют четких критериев, они отличаются во многих учреждениях. До апреля 2018 г. в клинических отделениях Института неонатологии и педиатрии НМИЦ АГП им. акад. В.И. Кулакова трансфузии донорских ЭСК крови проводились согласно внутреннему протоколу отделения реанимации и интенсивной терапии новорожденных: при потребности в искусственной вентиляции легких (ИВЛ) с уровнем среднего давления в дыхательных путях (mean airway pressure, МАР) > 8 см Н2О, концентрацией подаваемого кислорода (Fi02) > 0,4 и уровнем Ht венозной крови < 35%; ИВЛ с МАР < 8 см Н2О или неинвазивной вентиляции легких и Fi02 < 0,4 и значениях венозного Ht < 30%; при венозном Ht < 25% и отсутствии потребности в ИВЛ, но сохраняющейся зависимости в кислороде или потребности в неинвазивной респираторной терапии в возрасте старше 28 суток жизни плюс один или несколько из следующих симптомов: сохраняющейся > 24 ч тахикардии (частота сердечных сокращений > 180 уд/мин) или тахипноэ (частота дыхательных движений > 80/мин); повышении потребности в дополнительном кислороде
- 10%; прибавке массы тела < 10 г/кг/сут в течение 4 дней, несмотря на калорийность питания
- 100 ккал/кг/сут; учащении эпизодов апноэ; повышении лактата > 2,5 ммоль/л. Значения венозного Ht < 20% являлось абсолютным показанием для проведения гемотрансфузии.
С апреля 2018 г. в клинических отделениях Института неонатологии и педиатрии трансфузии донорских ЭСК крови начали проводить согласно рестриктивной стратегии [5].
Рисунок 1. Формирование выборки новорожденных детей, включенных в исследование
Figure 1. A flowchart of patient enrollment
Учитывая, что дети получали лечение в клинических отделениях одного учреждения, тактика проводимой терапии между исследуемыми группами не отличалась. Всем новорожденным при отсутствии противопоказаний проводилось сцеживание или отсроченное пережатие пуповины в родильном блоке по схожей методике. Все дети получали препараты рекомбинантного человеческого эритропоэтина эпоэтина альфа согласно инструкции в целях профилактики и лечения анемии у недоношенных новорожденных по схеме после 3-го дня жизни в дозе 200 МЕ/кг 3 раза/нед подкожно или внутривенно в течение первых 3-4 недель жизни. Длительность терапии рекомбинантным человеческим эритропоэтином во всех группах не отличалась. В течение периода госпитализации все дети получали препараты трехвалентного железа перорально в дозе 4-6 мг/кг/сут с момента достижения объема энтерального питания 100 мл/кг/сут. После выписки из стационара продолжалась терапия препаратами трехвалентного железа при наличии показаний под контролем уровней гемоглобина, эритроцитов и ферритина в крови. В случае снижения уровня ферритина в крови менее 35 мкг/л дозу препаратов железа увеличивали до 3-4 (максимум до 6) мг/кг/сут на ограниченный период. При повышении уровня ферритина в крови более 300 мкг/л терапию препаратами железа прекращали до снижения данного показателя до уровня ниже 300 мкг/л [10].
Проанализированы масса-ростовые параметры при рождении, гестационный возраст (ГВ), оценка по шкале Апгар на 1-й и 5-й минутах жизни, пол, частота антенатальной профилактики респираторного дистресс-синдрома, отсроченного пережатия/сцеживания пуповины, врожденной анемии, полицитемии; возраст проведения первой трансфузии донорских ЭСК крови, частота и общий объем трансфузий донорских ЭСК крови, длительность терапии препаратами железа после выписки, вид вскармливания в течение периода госпитализации и после выписки, сроки введения прикорма в исследуемых группах. При проведении смешанного или искусственного вскармливания выбор смеси формировался на основе оценки антропометрических показателей, нутритивного статуса детей.
Диагноз РН устанавливался согласно международной классификации, БЛД - согласно критериям A.H. Jobe и E. BancaLari в СВ 36 недель [11], НЭК - по клинико-лабораторным и инструментальным критериям по BeLL, ВЖК - согласно классификации, предложенной Российской ассоциацией специалистов перинатальной медицины.
Статистический анализ
Статистическая обработка данных выполнена с помощью электронных таблиц Microsoft Excel и программы SPSS v.17.0. Перед проведением сравнительного анализа количественных данных в исследуемых группах проверяли соответствие нормальному распределению (тест Колмогорова-Смирнова, графический анализ данных). Учитывая отсутствие нормального распределения данных, для количественных параметров определены медиана (Ме), значения 25-го и 75-го квартилей (IQR), для качественных данных - показатели частоты (%); для сравнения данных в группах применяли тест Манна-Уитни. Значимость различий между исходами проводилась с помощью критерия с2 и критерия Фишера. Статистически значимыми считались различия при р < 0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
ГВ детей составил от 24 до 28 недель. Анализируемые данные пациентов представлены в таблице 1.
Исследуемые группы статистически значимо не различались по ГВ, массе, длине тела при рождении, оценке по шкале Апгар на 1-й и 5-й минутах жизни (таблица 1). Частота врожденной анемии, полицитемии между группами не отличалась. Проведения частичной обменной трансфузии ни в одной группе не потребовалось.
Между исследуемыми группами выявлены статистически значимые отличия в возрасте проведения 1-й трансфузии, частоте, общем объеме и количестве трансфузий донорских ЭСК крови в течение периода госпитализации и уровне гемоглобина при выписке (таблица 2). В группе либеральной стратегии трансфузии донорских ЭСК крови потребовали 136/164 (82,9%) детей против 149/216 (68,9%) в группе рестриктивной стратегии, отношение шансов = 2,2 (95% доверительный интервал 1,3-3,6); Ме объема переливания составила 29,3 мл/кг (IQR 17,5-51,8 мл/кг) против 19,5 мл/кг (IQR 15,0-29,5 мл/кг) соответственно. Таким образом, возраст проведения 1-й трансфузии был более ранним в 1-й группе детей, общие количество и объем трансфузий за период госпитализации были больше в 1-й группе по сравнению со 2-й. Уровень гемоглобина при выписке был ниже во 2-й группе по сравнению с 1-й (таблица 2).
Проведен сравнительный анализ таких исходов и осложнений, как БЛД, РН, ПВЛ, ВЖК, постгеморрагическая гидроцефалия, НЭК у исследуемых групп детей при выписке из стационара (рисунок 2).
Статистически значимых отличий в частоте БЛД, в том числе тяжелой формы, ПВЛ, ВЖК > II степени в исследуемых группах не выявлено. Частота НЭК > II степени во 2-й группе по сравнению с 1-й группой была выше, отношение шансов = 1,6 (95% доверительный интервал 1,1-2,6), р = 0,034.
Сравнительный анализ частоты развития и тяжести анемии после выписки в исследуемых группах пациентов представлен в таблице 3.
Сравнительный анализ показал, что частота анемии после выписки была выше во 2-й группе по сравнению с 1-й в СВ 1 и 3 месяца (таблица 3). Все случаи анемии были железодефицитные. Тяжелой анемии после выписки не наблюдалась ни в одной группе.
Уровень сывороточного ферритина у детей в течение 6 месяцев жизни представлен в таблице 4.
Как видно из данных, представленных в таблице 4, Ме уровня ферритина в обеих группах соответствовала возрастной норме. У части детей отмечалось снижение уровня ферритина в крови менее рекомендуемых значений, в связи с чем увеличивали дозу препаратов железа до 3-4 мг/кг/сут (максимум до 6 мг/кг/сут) на ограниченный период с последующим контролем. Более длительная продолжительность терапии препаратами железа после выписки отмечалась во 2-й группе по сравнению с 1-й (Me (IQR) 4 (3-5,5) месяца и 3 (2-4) месяца соответственно, р = 0,002).
Таблица 1. Данные пациентов, включенных в исследование
Table 1. Data of the enrolled patients
Параметр Parameter | 1-я группа (либеральная стратегия;n = 164) Group 1 (liberal strategy; n= 164) | 2-я группа (рестриктивная стратегия; n = 216) Group 2 (restrictive strategy; n = 216) | P |
Антенатальная профилактика респираторного дистресс-синдрома, n (%) Antenatal prevention of respiratory distress syndrome, n (%) | 111 (67,7) | 166 (76,8) | 0,118 |
Отсроченное пережатие/сцеживание пуповины, n (%) Delayed umbilical cord clamping/milking, n (%) | 1431 (79,8) | 175 (81,0) | 0,332 |
ГВ, Me (IQR), недели GA, Me (IQR), weeks | 26,0 (25,0-28,0) | 25,5 (24,2-27,5) | 0,997 |
Масса при рождении, Me (IQR), г Birth weight, Me (IQR), g | 625 (480-900) | 620 (493-714) | 0,975 |
Длина тела при рождении, Me (IQR), см Birth length, Me (IQR), cm | 31 (28-33) | 30 (28-33) | 0,593 |
Шкала Апгар, 1-я минута, Me (IQR), баллы Apgar score at 1 minute, Me (IQR) | 4(2-5) | 3 (1-5) | 0,110 |
Шкала Апгар, 5-я минута, Me (IQR), баллы Apgar score at 5 minutes, Me (IQR) | 6(5-7) | 5 (4-7) | 0,069 |
Мужской пол, n (%) Male, n (%) | 88 (53,6) | 133 (61,6) | 0,128 |
Врожденная анемия, n (%) Congenital anemia, n (%) | 6 (3,6) | 8 (3,7) | 0,209 |
Полицитемия, n (%) Polycythemia, n (%) | 5 (3,0) | 5 (2,3) | 0,111 |
Таблица 2. Оценка возраста, общего объема и частоты трансфузий донорских ЭСК в исследуемых группах
Table 2. An analysis of age, total volume and frequency of donor red-cell transfusions in the study groups
Параметр Parameter | 1-я группа (либеральная стратегия;n = 164) Group 1 (liberal strategy; n= 164) | 2-я группа (рестриктивная стратегия;n = 216) Group 2 (restrictive strategy; n = 216) | P |
Дети, потребовавшие проведения трансфузии донорских ЭСК крови, n (%) Patients in need of a donor red-cell transfusion, n (%) | 136 (82,9) | 149 (68,9) | 0,024* |
Возраст 1-й трансфузии донорских ЭСК крови, Me (IQR), сутки жизни Age of the 1st donor red-cell transfusion, Me (IQR), days of life | 7 (3-13) | 10 (6-21) | 0,041* |
Количество трансфузий донорских ЭСК крови в течение госпитализации, Me (IQR) The number of donor red-cell transfusions during the hospital stay, Me (IQR) | 3(2-5) | 2(1-4) | 0,037* |
Общий объем трансфузий донорских ЭСК крови за период госпитализации на 1 ребенка, Me (IQR), мл/кг The total volume of donor red-cell transfusions during the hospital stay per 1 infant, Me (IQR), mL/kg | 29,3 (17,5-51,8) | 19,5 (15,0-29,5) | 0,035* |
Гемоглобин при выписке, Me (IQR), г/л Hemoglobin levels at discharge, Me (IQR), g/L | 109 (100-129) | 95 (88-113) | 0,006* |
Вид вскармливания в течение периода госпитализации и после выписки, сроки введения прикорма в исследуемых группах представлены в таблице 5.
Как видно из данных, представленных в таблице 5, в течение периода госпитализации частота исключительно грудного вскармливания во 2-й группе была выше, чем в 1-й, значения р приближены к статистически значимым. Большинство детей как на этапе госпитализации, так и после выписки получали смешанное вскармливание. Не выявлено отличий между группами по срокам введения прикорма.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ ИССЛЕДОВАНИЯ
В проведенном исследовании выявлено, что частота развития анемии на момент выписки из стационара, а также после (в СВ 1 и 3 месяца жизни) выше в группе детей, которым проводились трансфузии донорских ЭСК крови по рестриктивной стратегии в отличие от либеральной. Случаев тяжелой анемии после выписки ни в одной группе не обнаружено. После СВ 6 месяцев частота анемии значительно снижалась в обеих группах, что, с высокой вероятностью, связано с рационально проводимой антианемической терапией, своевременным введением прикорма.
Рисунок 2. Сравнительный анализ частоты БЛД, РН, ПВЛ, ВЖК, постгеморрагической гидроцефалии, НЭК у пациентов при разных стратегиях трансфузии донорских ЭСК крови (%)
Figure 2. A comparative analysis of the incidence of BPD, ROP, PVL, IVH, posthemorrhagic hydrocephalus, NEC in the patients in different strategies of red-cell transfusion (%)
ROP - retinopathy of prematurity; NEC - necrotizing enterocolitis; PVL - periventricular leukomalacia; BPD - bronchopulmonary dysplasia; IVH - intraventricular hemorrhage
Таблица 3. Сравнительный анализ частоты развития анемии после выписки в исследуемых группах
Table 3. A comparative anaLysis of incidence of anemia after discharge in the study groups
Параметр Parameter | 1-я группа (либеральная стратегия;n = 164) Group 1 (liberal strategy; n= 164) | 2-я группа (рестриктивная стратегия; n = 216) Group 2 (restrictive strategy; n = 216) | Отношение шансов (95% доверительный интервал) Odds ratio (95% confidence Interval) | P |
Частота анемии в СВ 1 месяц, n (%) Anemia incidence at a CA of 1 month, n (%) | 32 (44,4) | 106 (63,8) | 2,2 (1,3-3,9) | 0,026* |
Частота анемии в СВ 3 месяца, n (%) Anemia incidence at a CA of 3 months, n (%) | 28 (38,9) | 90 (54,2) | 1,8 (1,1-3,3) | 0,042* |
Частота анемии в СВ 6 месяцев, n (%) Anemia incidence at a CA of 6 months, n (%) | 18 (25,0) | 27 (16,3) | 0,6 (0,3-1,1) | 0,149 |
Частота анемии в СВ 12 месяцев, n (%) Anemia incidence at a CA of 12 months, n (%) | 1 (1,4) | 0 | - | - |
Частота анемии в СВ 18 месяцев, n (%) Anemia incidence at a CA of 18 months, n (%) | 1 (1,4) | 0 | - | - |
Частота анемии в СВ 24 месяца, n (%) Anemia incidence at a CA of 24 months, n (%) | 1 (1,4) | 0 | - | - |
Таблица 4. Уровень ферритина в сыворотке крови у детей в исследуемых группах в течение 6 месяцев жизни
Table 4. Serum ferritin levels in the study groups within 6 months of corrected age
Параметр Parameter | 1-я группа (либеральная стратегия; n = 72) Group 1 (liberal strategy; n = 72) | 2-я группа (рестриктивная стратегия; n = 166) Group 2 (restrictive strategy; n = 166) | P |
Уровень ферритина в сыворотке крови, 1 месяц, Me (IQR), мкг/л Serum ferritin levels, 1 month of CA, Me (IQR), pg/L | 62 (40-82) | 51 (38-57) | 0,126 |
Уровень ферритина в сыворотке крови, 3 месяца, Me (IQR), мкг/л Serum ferritin levels, 3 months of CA, Me (IQR), pg/L | 32 (20,5-55,5) | 25 (21-28,5) | 0,287 |
Уровень ферритина в сыворотке крови, 6 месяцев, Me (IQR), мкг/л Serum ferritin levels, 6 months of CA, Me (IQR), pg/L | 16 (12-25) | 17,5 (12-23) | 0,188 |
Таблица 5. Вид вскармливания в течение периода госпитализации и после выписки, сроки введения прикорма в исследуемых группах
Table 5. Type of feeding during the hospital stay and after discharge and timing of weaning in the study groups
Вид вскармливания Type of feeding | 1-я группа (либеральная стратегия) Group 1(liberal strategy) | 2-я группа (рестриктивная стратегия) Group 2 (restrictive strategy) | р |
В течение периода госпитализации During the hospital stay | (n = 164) | (n = 216) |
|
Исключительно грудное вскармливание, n (%) Exclusive breastfeeding, n (%) | 49 (29,9) | 75 (34,7) | 0,071 |
Смешанное вскармливание, n (%) Mixed feeding, n (%) | 89 (54,3) | 100 (46,3) | 0,473 |
Искусственное вскармливание, n (%) Formula feeding, n (%) | 26 (15,8) | 41 (19) | 0,362 |
После выписки After discharge | (n = 72) | (n = 166) |
|
Грудное вскармливание, n (%) Exclusive breastfeeding, n (%) | 12 (16,7) | 46 (27,7) | 0,085 |
Смешанное вскармливание, n (%) Mixed feeding, n (%) | 41 (56,9) | 77 (46,4) | 0,369 |
Искусственное вскармливание, n (%) Formula feeding, n (%) | 19 (26,4) | 43 (25,9) | 0,819 |
Введение прикорма, Me (IQR), месяцы Age at weaning, Me (IQR), months | 6,5 (5,5-7) | 6(5-7) | 0,253 |
Известно, что длительные эпизоды гипоксемии у детей с очень низкой массой тела связаны с неблагоприятными долгосрочными исходами [12]. Доказывая свою позицию, сторонники либеральной стратегии трансфузий главным образом основываются на этом аргументе. В то же время в ряде исследований приводятся данные о том, что трансфузии донорских ЭСК крови ассоциированы с такими неблагоприятными исходами и осложнениями, как летальный исход [13], РН [14, 15], БЛД [16, 17], ВЖК [18, 19], НЭК [20].
В соответствии с наиболее крупными исследованиями: The Premature Infants in Need of Transfusion (PINT) [21], Effects of Liberal vs Restrictive Transfusion Thresholds on Survival and Neurocognitive Outcomes (ETTNO) и Transfusion of Prematures (TOP) (NCT01702805) [4] неонатальные исходы между группами недоношенных детей, получавших трансфузии по либеральной и рестриктивной стратегиям, существенно не отличались. В настоящей работе мы также сравнивали частоту БЛД, РН > II степени, ПВЛ, ВЖК > II степени, НЭК > III степени у недоношенных детей с ЭНМТ в группах либеральных и рестриктивных стратегий переливания донорских ЭСК крови. Повышения частоты анализируемых неонатальных исходов в группе рестриктивной стратегии за исключением НЭК > III степени не обнаружено. Патогенез НЭК является мультифакторным и для установления причин увеличения его частоты во 2-й группе требуется дополнительный анализ, что не являлось непосредственной целью данного исследования. Полученные результаты позволяют утверждать об отсутствии прямой причинно-следственной ассоциации между проведением гемотрансфузий и развитием описанных осложнений и исходов у недоношенных новорожденных, по крайней мере, в рамках 2 сравниваемых стратегий трансфузий. Высокая частота анемии и потребность в проведении гемотрансфузии с высокой вероятностью отражают тяжесть состояния крайне недоношенных детей. Важным является тот факт, что использование более низких пороговых значений для переливания крови сокращает количество трансфузий.
В большинстве РКИ, посвященных сравнению 2 стратегий трансфузии, конечными точками являются оценки неврологических исходов. Сведения о частоте анемии у детей после выписки в вышеописанных РКИ отсутствуют. Поэтому мы не можем сопоставить полученные нами результаты. Частота анемии после выписки была относительно невысокой. В СВ 1 месяц она встречалась у 32/72 (44,4) детей в группе либеральной тактики против 106/166 (63,8) - в группе рестриктивной, р = 0,026, в СВ 3 месяца - у 28 (38,9) в группе либеральной стратегии против 90 (54,2) - в группе рестриктивной, р = 0,042, после СВ 6 месяцев она значительно снижалась, и отличий между группами до СВ 24 месяца жизни не наблюдалось.
Многократные гемотрансфузии могут сопровождаться увеличением уровня ферритина в сыворотке крови и приводить к перегрузке железом. По результатам нашего исследования уровень сывороточного ферритина у детей в течение 6 месяцев жизни между группами не отличался. Тем не менее отмечалось более высокое содержание ферритина в 1-й группе в первые 3 месяца СВ. Также интересен и тот факт, что в группе либеральной стратегии повышения уровня ферритина в крови более 300 мкг/л и признаков перегрузки железом не встречалось. Длительность терапии препаратами железа после выписки была достоверно продолжительнее во 2-й группе по сравнению с 1-й. Это может быть связано, с одной стороны, с повторным использованием организмом железа, полученного при разрушении перелитых эритроцитов в 1-й группе, и тем, что во 2-й группе частота исключительно грудного вскармливания как на этапе госпитализации, так и после выписки была выше. Согласно рекомендациям, детям, находящимся на грудном вскармливании и не получающим обогатитель грудного молока, необходимо получать дотацию препаратами трехвалентного железа до 6 месяцев или до введения прикорма или смесей, обогащенных железом, что соответствует нашим данным. В то время как дети, получающие специализированную смесь для недоношенного ребенка или обогатитель грудного молока и имеющие нормальный уровень железа и ферритина в крови, не нуждаются в дополнительной дотации препаратов трехвалентного железа.
Исходя из полученных нами результатов, а также данных РКИ, можно сделать вывод о том, что рестриктивные стратегии трансфузии донорских ЭСК крови столь же безопасны, как и либеральные. Безусловно, РКИ выполняют важную задачу в доказательной медицине, тем не менее следует обратить внимание на следующие моменты. При детальном изучении данных РКИ выявляется, что зачастую они проводятся среди достаточно разнородной когорты
пациентов, а выводы не всегда корректно толкуются. Поверхностно ознакомившись с рекомендациями по рестриктивной стратегии трансфузий, легко предположить следующее: рестриктивная практика применима ко всем недоношенным детям, она не повышает риски неблагоприятных исходов по сравнению с более либеральными стратегиями и, следовательно, от либеральной практики следует воздерживаться, когда есть какие-либо сомнения в ее пользе. Эти предположения можно рассматривать как логичные выводы, за исключением случаев, когда тщательный анализ имеющихся данных исследований диктует иное. Коррекцию анемического синдрома у пациента необходимо проводить с учетом комплексной оценки клинической картины и данных дополнительных лабораторно-инструментальных исследований. В частности, в случаях крупных хирургических вмешательств, необходимости проведения экстракорпоральной мембранной оксигенации, кардиореспираторных заболеваний (пороки сердца, БЛД, шок), сепсиса, кровотечений или симптомов, присущих анемии (тахикардия, тахипноэ) не рекомендуется применять рестриктивные стратегии трансфузий. В этих случаях оптимальный критерий для проведения трансфузии в настоящее время остается малоизученным. Решение о трансфузии донорских ЭСК крови должно иметь персонализированный подход, оценивая как пользу, так и риски.
Ограничения исследования
Наше исследование имеет ряд ограничений. Во-первых, оно является одноцентровым, что обусловлено различиями применяемых технологий при выхаживании глубоко недоношенных детей в медицинских учреждениях нашей страны, в частности отличиями в пороговых значениях гемоглобина при гемотрансфузиях донорских ЭСК крови до утверждения клинических рекомендаций по анемиям у недоношенных детей. Во-вторых, исследование было ретроспективным, отсутствует рандомизация пациентов, так как проводился сравнительный анализ с учетом исторически сложившейся тактики. Также в связи с ретроспективным анализом проведенного исследования недостатком его являлось отсутствие таких дополнительных лабораторных данных у детей, как уровень ретикулоцитов, содержание гемоглобина в них. Тем не менее настоящая работа дополняет существующие данные о неонатальных исходах и является единственной, где представлены сведения о частоте развития анемии после выписки из стационара у недоношенных детей с ЭНМТ, которым проводились трансфузии по рестриктивной и либеральной стратегиям.
ЗАКЛЮЧЕНИЕ
Результаты проведенного анализа демонстрируют, что применение рестриктивной стратегии гемотрансфузии не приводит к клинически значимому увеличению частоты таких исходов, как РН > III степени, БЛД, ПВЛ, ВЖК > II степени, а также анемии после 6 месяцев жизни в изучаемой группе недоношенных детей с ЭНМТ. Частота НЭК > II степени в группе рестриктивной стратегии была выше, что требует дополнительного анализа.
ИСТОЧНИК ФИНАНСИРОВАНИЯ
Не указан.
КОНФЛИКТ ИНТЕРЕСОВ
Авторы статьи подтвердили отсутствие конфликта интересов, о котором необходимо сообщить.
Об авторах
Дияна Рашидовна Шарафутдинова
ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова» Минздрава России; ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Сеченовский Университет)
Email: dikarush@gmail.com
ORCID iD: 0000-0001-9626-5481
канд. мед. наук
Россия, Москва; МоскваЕкатерина Николаевна Балашова
ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова» Минздрава России
Email: katbal99@gmail.com
ORCID iD: 0000-0002-3741-0770
канд. мед. наук
Россия, МоскваАнна Александровна Пучкова
ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова» Минздрава России
Email: annapuchkova@mail.ru
ORCID iD: 0000-0001-6897-247X
канд. мед. наук
Россия, МоскваАнна Владимировна Дегтярева
ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова» Минздрава России; ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Сеченовский Университет)
Email: a_degtyareva@oparina4.ru
ORCID iD: 0000-0003-0822-751X
д-р мед. наук, профессор
Россия, Москва; МоскваАнна Ревазиевна Киртбая
ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова» Минздрава России; ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Сеченовский Университет)
Email: a_kirtbaya@oparina4.ru
ORCID iD: 0000-0002-7628-8157
д-р мед. наук, профессор
Россия, Москва; МоскваРуфина Анваровна Лутфуллина
ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова» Минздрава России
Email: rufinalutfullina@gmail.com
ORCID iD: 0009-0003-7186-1182
Россия, Москва
Тамара Курейшевна Цечоева
ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова» Минздрава России
Email: kim_ka_ts@mail.ru
ORCID iD: 0000-0001-5985-3540
Россия, Москва
Анна Андреевна Козловская
ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова» Минздрава России
Автор, ответственный за переписку.
Email: noreply@eco-vector.ru
ORCID iD: 0009-0001-2541-3667
Россия, Москва
Олег Вадимович Ионов
ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова» Минздрава России; ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Сеченовский Университет)
Email: o_ionov@oparina4.ru
ORCID iD: 0000-0002-4153-133X
д-р мед. наук, профессор
Россия, Москва; МоскваСписок литературы
- Franz A.R., Engel C., Bassler D., Rüdiger M., Thome U.H., Maier R.F., et al. ETTNO Investigators. Effects of liberal vs restrictive transfusion thresholds on survival and neurocognitive outcomes in extremely low-birth-weight infants: the ETTNO randomized clinical trial. JAMA 2020; 324 (6): 560–70.
- Colombatti R., Sainati L., Trevisanuto D. Anemia and transfusion in the neonate. Semin Fetal Neonatal Med 2016; 21 (1): 2-9.
- Holzapfel L.F., Rysavy M.A., Bell E.F. Red blood cell transfusion thresholds for anemia of prematurity. Neoreviews 2023; 24 (6): 370–6.
- Kirpalani H., Bell E.F., Hintz S.R. Eunice Kennedy Shriver NICHD Neonatal Research Network. Higher or lower hemoglobin transfusion thresholds for preterm infants. N Engl J Med 2020; 383 (27): 2639–51.
- Балашова Е.Н., Шарафутдинова Д.Р., Нароган М.В., Пучкова А.А., Дегтярева А.В., Сапун О.И. и др. Ранняя анемия недоношенных (клинические рекомендации). Неонатология: новости, мнения, обучение. 2021; 9 (3): 47–61.
- Dallman P.R. Anemia of prematurity. Annu Rev Med 1981; 32: 143–60.
- Girelli G., Antoncecchi S., Casadei A.M., Del Vecchio A., Isernia P., Motta M., et al. Recommendations for transfusion therapy in neonatology. Blood Transfus 2015; 13 (3): 484–97.
- Железодефицитная анемия у детей и подростков. Клинические рекомендации. [Электронный ресурс] URL: https://nodgo.org/sites/default/files/ЖДА%20%28альтернативная%20версия%29.pdf. (дата обращения 03.06.2025)
- World Health Organization: Haemoglobin concentrations for the diagnosis of anaemia and assessment of severity. Vitamin and Mineral Nutrition Information System. Geneva: World Health Organization; 2011. [Electronic resource] URL: https://
- www.who. int / vmnis/indicators/haemoglobin.pdf. Accessed 29 Mar 2015.
- Domellöf M. Meeting the iron needs of low and very low birth weight infants. Ann Nutr Metab 2017; 71 (3): 16–23.
- Jobe A.H., Bancalari E. Bronchopulmonary dysplasia. Am J Respir Crit Care Med 2001; 163 (7): 1723–9.
- Poets C.F., Roberts R.S., Schmidt B. Canadian Oxygen Trial Investigators. Association between intermittent hypoxemia or bradycardia and late death or disability in extremely preterm infants. JAMA 2015; 314 (6): 595–603.
- Dos Santos A.M., Guinsburg R., de Almeida M.F., Procianoy R.S., Rodrigues Leone C., Martins Marba S.T., et al; Brazilian Network on Neonatal Research. Red blood cell transfusions are independently associated with intra-hospital mortality in very low birth weight preterm infants. J Pediatr 2011; 159 (3): 371–6.
- Slidsborg C., Jensen A., Forman J.L., Rasmussen S., Bangsgaard R., Callø Fledelius H., et al. Neonatal risk factors for treatment-demanding retinopathy of prematurity: a Danish national study. Ophthalmology 2016; 123 (4): 796–803.
- Inder T.E., Clemett R.S., Austin N.C., Graham P., Darlow B.A. High iron status in very low birth weight infants is associated with an increased risk of retinopathy of prematurity. J Pediatr 1997; 131 (4): 541–4.
- Valieva O.A., Strandjord T.P., Mayock D.E., Juul S.E. Effects of transfusions in extremely low birth weight infants: a retrospective study. J Pediatr 2009; 155 (3): 331–7.
- Ghirardello S., Dusi E., Cortinovis I., Villa S., Fumagalli M., Agosti M., et al. Effects of red blood cell transfusions on the risk of developing complications or death: an observational study of a cohort of very low birth weight infants. Am J Perinatol 2017; 34 (1): 88–95.
- Christensen R.D., Baer V.L., Del Vecchio A., Henry E. Unique risks of red blood cell transfusions in verylow-birth-weight neonates: associations between early transfusion and intraventricular hemorrhage and between late transfusion and necrotizing enterocolitis. J Matern Fetal Neonatal Med 2013; 26 (2): 60–3.
- Baer V.L., Lambert D.K., Henry E., Snow G.L., Butler A., Christensen R.D. Among very-low-birthweight neonates is red blood cell transfusion an independent risk factor for subsequently developing a severe intraventricular hemorrhage? Transfusion 2011; 51 (6): 1170–8.
- Mohamed A., Shah P.S. Transfusion associated necrotizing enterocolitis: a meta-analysis of observational data. Pediatrics 2012; 129 (3): 529–40.
- Whyte R.K., Kirpalani H., Asztalos E.V., Andersen C., Blajchman M., Heddle N., et al; PINTOS Study Group. Neurodevelopmental outcome of extremely low birth weight infants randomly assigned to restrictive or liberal hemoglobin thresholds for blood transfusion. Pediatrics 2009; 123 (1): 207–13.
Дополнительные файлы